(Foto: Lillian Suwanrumpha/AFP)
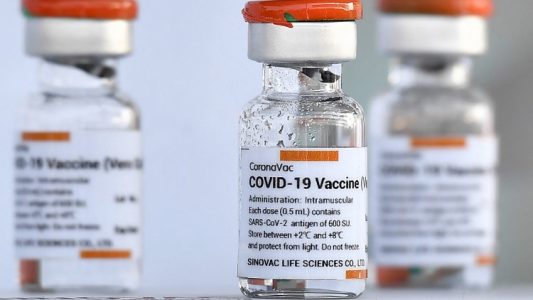
A Agência Nacional de Vigilância Sanitária (Anvisa) interditou preventivamente 25 lotes da vacina CoronaVac. A decisão veio no sábado (4) e afeta um total de 12 milhões de doses no Brasil. A medida é cautelar, ou seja, não é punitiva e busca apenas precaver o uso de vacinas produzidas em um laboratório não inspecionado pela Agência.
Nesse sentido, a decisão tem validade de 90 dias. De acordo com a Anvisa, o Instituto Butantan relatou que a unidade fabril responsável pelo envase não foi inspecionada e não foi incluída na autorização de uso emergencial da vacina. Ou seja, são considerados produtos não regularizados pela Agência.
“Foi o próprio Instituto que, por compromisso com a transparência e por extrema precaução, comunicou o fato à agência, após atestar a qualidade das doses recebidas. Isso garante que os imunizantes são seguros para a população”, diz a nota oficial do Butantan.